

复旦大学附属肿瘤医院病理科李媛主任团队与复星杏脉合作的科研论文A new AI-assisted scoring system for PD-L1 expression in NSCLC (人工智能辅助非小细胞癌(NSCLC)PD-L1表达评分系统),获得国际权威期刊Computer Methods and Programs in Biomedicine(CMPB,影响因子7.03, JCR:Q1区)发表。CMPB涵盖了源自计算科学的计算方法和软件系统,用于在生物医学研究和医学实践的各个方面实施。

肺癌是世界范围内死亡率第一的恶性肿瘤,其中非小细胞肺癌占85%。【1】
全国肿瘤登记中心2022年发布数据显示:2020年我国新发肺癌病例81万,占中国新确诊癌症人数的17.9%。
有效筛选PD-1/PD-L的潜在获益人群,为PD-1抗体实现免疫治疗的关键,肿瘤细胞通过高表达的PD-L1与T细胞表面PD-1结合,抑制T细胞引发的免疫效应,实现免疫逃逸。截至目前,三种针对PD-1的药物,通过FDA的批准在美国以及其它国家上市用于癌症治疗。其中两种(O药和K药)已经获批在国内上市。
PD-1/PD-L1抑制剂在临床实践面临问题包括:治疗周期长,费用高, 其中相关研究显示约20%的患者获益[2]。 国内外对PD-L1的蛋白表达主要采用免疫组化检测,PD-L1表达水平可作为一种免疫治疗预测及预后标志物,用于筛选免疫治疗的潜在获益人群及预测免疫治疗疗效,因此,准确可靠的PD-L1判读及判读结果对筛选优势人群尤为重要。
近年来,免疫治疗已成为NSCLC患者的一种有效的治疗方式。程序性死亡-配体1(PD-L1)为NSCLC免疫检查点之一,对于肿瘤细胞阳性比例评分(TPS,注:TPS=PD-L1膜染色阳性肿瘤细胞数/总肿瘤细胞数*100%)的准确评估仍然具有挑战性。传统的病理医生视觉评估大多采用估值方式,无法完整计算整张玻片上的所有肿瘤细胞数目,导致诊断的结果不够精准,无法进一步与治疗方式进行更加紧密的关联研究,而且病理医生的判断主观性较强、个体差异较大。
AI辅助的数字化病理诊断就可以帮助病理医生来降低这种主观因素导致的个体之间的一致性差异,可以帮助他们做出更好的治疗决策。最近,各种类型的研究已经证明了基于深度学习的方法能够自动评估TPS。但是,目前的方法仍存在两方面的不足。首先,由于训练具有竞争力的深度神经网络模型依赖于大规模、高质量的标注数据,之前的绝大部分的标注都是在patch水平或者Field of view水平上进行的。另外,参加与AI辅助评分系统比较的病理学家人数最多仅 5 人,可能导致对比实验结果的可信度不高,需要更多的病理学家进行更丰富的比较。
在本研究中,我们开发了一种基于深度学习方法用于NSCLC PD-L1表达评估。我们是基于全视野数字病理切片(Whole Slide Imges,WSIs)执行的更广泛的标注,其中训练集包含 37308 个PD-L1阳性肿瘤细胞(TC)和 43427 个PD-L1阴性TC,测试集包含115个WSIs。金标准TPS 由两位具有 PD-L1 TPS评分认证的病理学专家评估,不一致的病例由第三位病理学专家顾问审查。与此同时,将AI的评分结果与11名病理医生(5名经验丰富的和6名缺乏经验的病理医生)进行了比较。
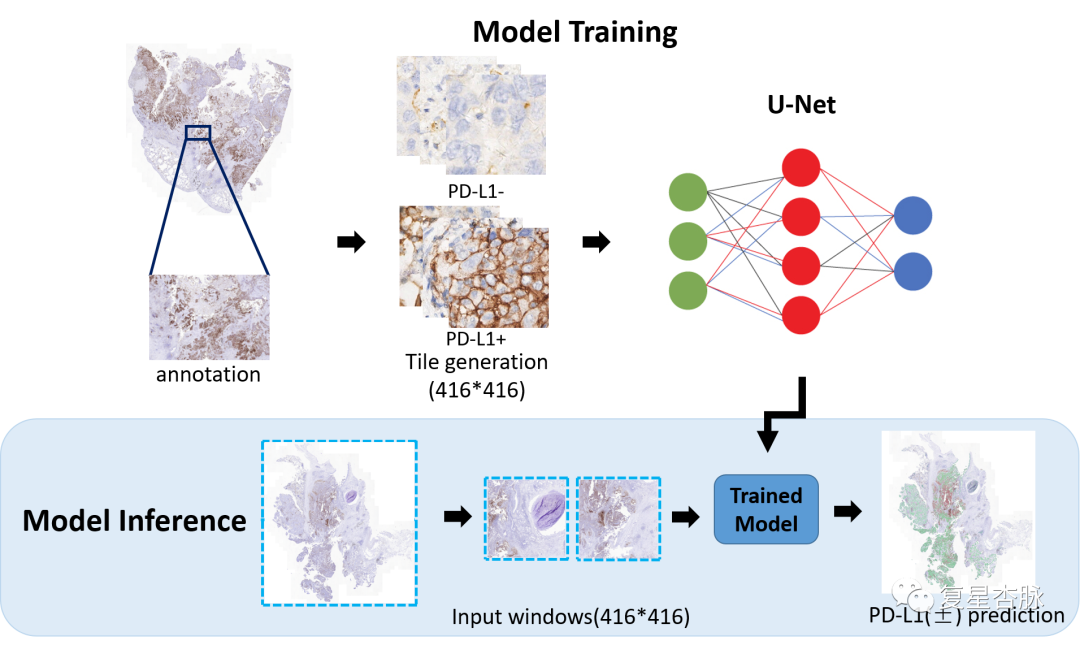
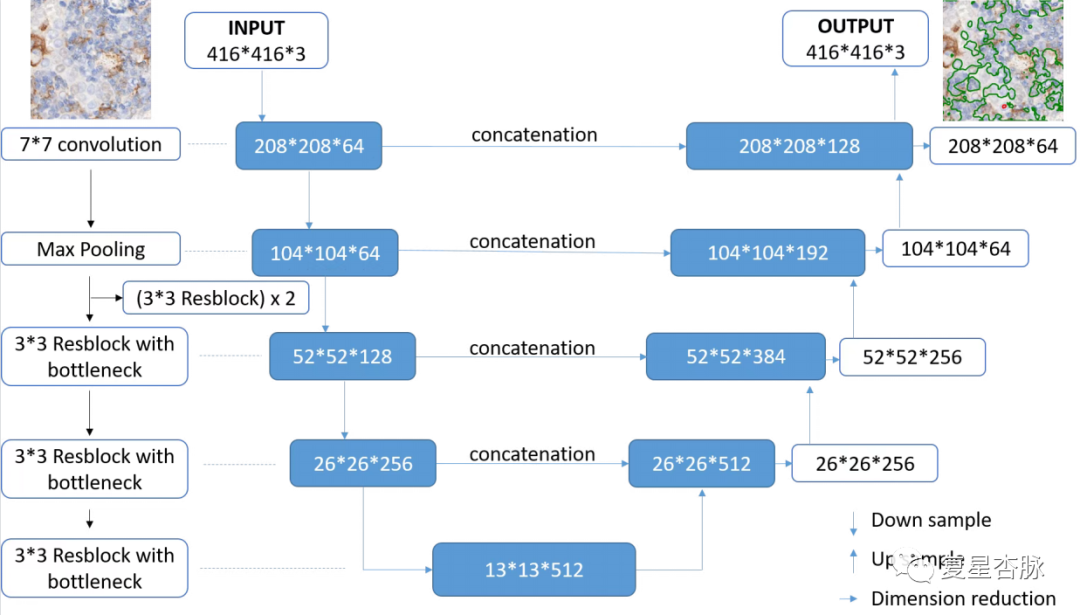
在本研究中, 我们采用一种新的人工智能辅助评分系统用于评估NSCLC PD-L1表达。我们将免疫组化(IHC)图像的标注区域被平铺成不重叠的patch(416 × 416 像素),使用 U-net 上采样和下采样将细胞轮廓、细胞核等低级特征与正负TC分类的高级特征相结合。此外,相比较传统的 U-net 架构,我们添加了 res-blocks,可以提高提取特征的能力并解决训练过程中梯度消失的问题。为了确定 WSI 的 TPS 值,我们提出了如下 3 步方法:(1)分割 WSI 每个patch的阳性和阴性肿瘤细胞; (2)计算阳性和阴性肿瘤细胞的面积,并将这些面积相加,计算出WSI的TPS值; (3) 使用 TPS 计算公式来确定 WSI的TPS 值。
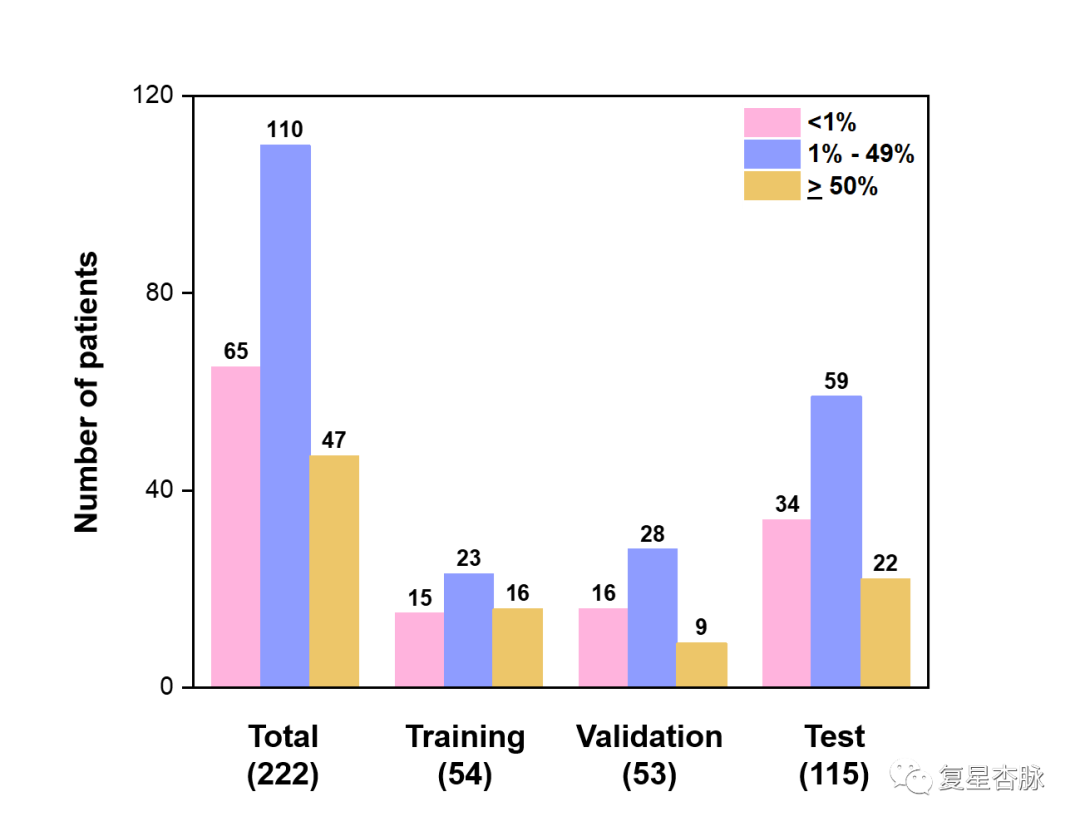
我们入组了2017 年 9 月至 2020 年 12 月期间被确诊为 NSCLC的222名患者,训练、验证、测试集分别为54、53、115例病人,且每个数据集都包含不同级别的TPS诊断结果。
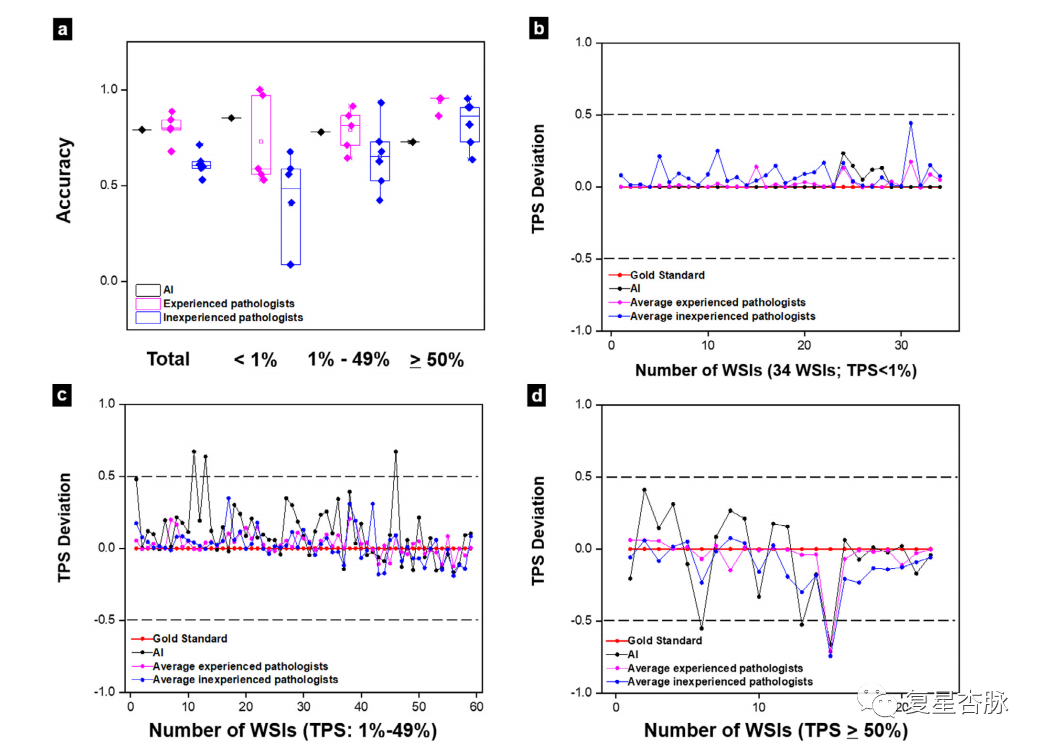
实验结果表明,在 TPS 阴性(TPS小于1%)子集中,AI的准确度最高(85.29%),优于经验丰富的病理学家(72.94%)和缺乏经验的病理学家(40.20%)。总体结果表明AI 模型在测试数据集中的表现优于低年资病理医生,接近高年资病理医生。使用基于细胞水平标注的模型训练和 11 名参与评估的病理医生表明我们的数据集覆盖范围更广,使得我们得模型更为可信。
研究团队开发的 Aitrox AI 模型在大多数 TPS 评分中的表现优于没有经验的病理医生,显示了模型在协助常规病理学家诊断、PD-L1评分具有很好的潜力。开发可应用于临床的Aitrox AI系统,以辅助病理医生的诊断工作具有重要的临床意义。同时在NSCLC的PD-L1的临床评分过程中,杏脉AI是有效的辅助评分工具。
复星杏脉目前与复旦大学附属肿瘤医院病理科开展了多项基础科学研究,双方始终坚信科研必须和临床紧密联系,深化创新,夯实基础研究,建设产学研一体化,AI应用场景得到落地。复旦肿瘤医院病理科是全国肿瘤病理最大的会诊中心,年会诊病例从2万例增长至4万例。70%的对外会诊病例来自于长三角地区,起到长三角“龙头”作用,解决了大量疑难病例的病理诊断。参与国内多个非小细胞肺癌及食管癌相关的指南与共识。近五年来,承担国家级及省部级等各类科研项目43项,科研经费合计5500余万元;发表SCI文章155篇。复星杏脉早在2019年“一致性系数94.6%”荣登国际权威全球病理竞赛CancerCellularityChallenge冠军榜首、并与2021-MICCAI-FLARE腹部多器官的分割任务中获得冠军。截至2022年6月发表及审稿中的AI临床前科研项目总计32项,累计SCI期刊影响因子总计336.2分,知识产权超过100余项,项创新项目成功获得国家重点研发计划、国家自然科学基金课题、上海市科委、经信委及发改委课题。

复星杏脉作为复星旗下首个独立孵化的人工智能企业,自2017年成立以来一直保持高速发展的趋势,团队已积累超过40种AI疾病模型储备,与全国500多家医疗机构达成合作。成熟应用已上线放射科、检验科、病理科、呼吸科、骨科、心内科、神经科等多个科室。复星杏脉作为复星“创新驱动”战略尖兵与医疗人工智能产业核心平台进行布局发展,通过“匠心+创新”,不断加大科技研发投入。
同时,复星杏脉深入医疗机构与基层健康服务场景探索真实需求,积极完善分级诊疗的核心场景服务能力如早筛、远程诊疗、精准医疗等,致力于全面解决不同的临床痛点和公卫难题。通过独树一帜的“AI+X”产品形态,有效赋能远程诊疗体系建设,形成了促进我国分级诊疗与精准医疗落地的有效解决方案。
[1]Herbst RS, Heymach JV, Lippman SM. Lung cancer[J]. N EnglJ Med, 2008, 360(13): 1367-1380. [2] Ma W, Gilligan BM, Yuan J. Current status and perspectives in translational biomarker research for PD-1/PD-L1 immune checkpoint blockade therapy. J Hematol Oncol. 2016 May 27;9(1):47. doi: 10.1186/s13045-016-0277-y.
“锐影”随行|上海长征医院联合复星杏脉通过人工智能区分肺部磨玻璃结节良恶性科研成果发表
“锐影”随行|上海长征医院联合复星杏脉使用多任务学习与深度影像组学对于肺部CT磨玻璃结节浸润性进行预测
